1. 引言
淫羊藿为小檗科(Berbridaceae)淫羊藿属(Epimedium)植物,全世界有40多个种,中国是本属植物最主要的分布区,共有27种及4个变种,约占世界总数的70% [1] 。2000年版《中华人民共和国药典》收载了同属植物淫羊藿、箭叶淫羊藿、柔毛淫羊藿、巫山淫羊藿和朝鲜淫羊藿5个种为正品干燥地上部分入药。
淫羊藿的主要活性成分包括黄酮类化合物、淫羊藿素等。目前淫羊藿种及其制剂的质量控制大多采用HPLC法,以检测淫羊藿苷(icariin)及其总黄酮为主要指标。淫羊藿的炮制方法有20余种,其中羊脂油拌炒法为历代一直沿用,多数采用羊脂油先加热熔化后再加入淫羊藿丝,用文火炒至均匀有光泽,取出放凉的炮制方法。当前研究发现,淫羊藿的药理作用主要有:促进蛋白合成 [2] [3] ;调节免疫系统 [4] ,增强抵抗力 [5] ;调节心脑血管系统,对脑缺血有保护作用 [6] ,抑制阻断双侧颈总动脉引起的血压升高 [7] ;抗衰老 [8] ;抗肿瘤 [9] ;提高性肌能增加性器官重量,提高性激素分泌量,治疗阳痿 [10] ;防治骨质疏松 [11] 。
近红外分析技术广泛应用在食品、烟酒、化学及中药领域,近红外光谱具有检测快、无损、绿色等特点 [12] 。它的快速性使其适用于实时监测生产过程,提高生产效率。无损检测意味着在分析样品时不需要破坏样品,这对于一些对样品保存有要求的应用非常重要。同时,近红外光谱技术能够同时提供化学和物理信息,使其在分析过程中更为全面 [13] 。不破坏样品可同时反馈化学和物理信息的这一优点,使其可用于开发过程在线监控模型 [14] 。在生产过程中使用近红外光谱技术建立模型,以实时监测和控制生产过程。这有助于在生产中及时发现问题、调整参数,并确保产品的质量符合要求。这对于提高生产效率、减少成本和确保产品一致性有很大帮助。
近红外光谱技术在制药工业中的应用逐渐扩展,不仅在药物的定性和定量分析方面发挥着重要作用,而且在生产过程的各个阶段(包括合成、制剂、包装等过程)的监控中展现出巨大的潜力 [15] [16] [17] 。2002年,美国FDA已将近红外光谱技术作为一种标准的检测方法。2005版《中国药典》将“近红外分光光度法指导原则”列入附录,进一步确认了该技术在药物领域的重要性。本研究采用近红外光谱技术结合偏最小二乘(PLS)化学计量学方法,对淫羊藿原药材进行了总黄酮的检测分析。通过建立定量分析模型,旨在提供一种新的、能够快速准确监控淫羊藿药材质量的方法,以支持后续直接的生产,确保淫羊藿原药材的质量符合要求。
2. 实验部分
2.1. 仪器与试剂
淫羊藿药材(华润三九股份有限公司);Antaris II近红外光谱仪(赛默飞世尔科技公司);ML203型电子天平(梅特勒–托利多公司);
甲醇(AR,广州化学试剂厂)。
2.2. 采集近红外漫反射光谱
淫羊藿药材光谱采集前的预处理:由华润三九股份有限公司技术部负责收集,共取样83批。
光谱采集条件:采集淫羊藿药材粉末(过5号筛)样品的漫反射光谱,光谱扫描范围4000~12000 nm,分辨率8 cm−1,见图1;实验采用内部参比进行光谱采集分析。
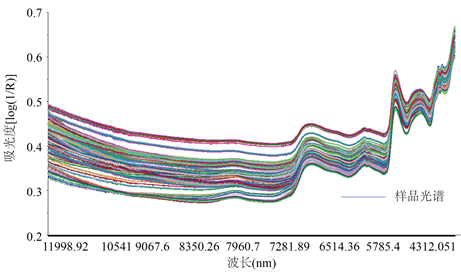
Figure 1. Near infrared original acquisition spectrum of Epimedium
图1. 淫羊藿药材近红外原始采集光谱
2.3. 测定淫羊藿药材总黄酮
精密称取淫羊藿药材提取的总黄酮0.5 ml,置50 ml量瓶中,加甲醇至刻度,摇匀,作为供试品溶液。另取淫羊藿苷对照品适量,精密称定,加甲醇制成每1 ml含10 μg的溶液,作为对照品溶液。分别取供试品溶液和对照品溶液,以相应试剂为空白,参照紫外–可见分光光度法(通则0401),在270 nm波长处测定吸光度,计算总黄酮得率,即得。
2.4. 数据处理
为了确保近红外光谱采集的稳定性和精确度,使用数据分析软件中常用的光谱预处理方法有:正交信号校正(OSC)、一阶导数(1st derivative)、二阶导数(2nd derivative)、去趋势化(detrend)、矢量归一化(SNV)等。可以有效降低外界环境及仪器状态带给样品近红外光谱之间的差异,确保近红外光谱包含了样品大量的有效信息。
光谱进行预处理结果后,通过MLR、PLS和SVR三种算法建立淫羊藿中总黄酮醇苷的定量模型,建立模型后,考察使用交叉验证法(Leave-One-Out Cross Validation, LOOCV)计算交叉验证均方根误差(RMSECV)。RMSECV越小越好,相关系数(R)趋近于1,模型预测效果好。RMSEC和RMSEP值差值越小越好。其中验证集相对偏差通常控制在10%内,数值越低越好。以上数据均用TQ软件进行计算。
3. 结果与讨论
3.1. 淫羊藿药材总黄酮含量测定结果
按照2.3项下的方法测定83批淫羊藿药材中总黄酮的含量,总黄酮含量的范围4.968%~19.265%之间。
3.2. 光谱预处理
本研究比较了不同预处理方法对淫羊藿药材中总黄酮含量建模的影响,最终选择矢量归一化(SNV)预处理方法对光谱进行处理,去除光谱背景中影响成分,减少变异性,结果如图2所示。

Figure 2. Spectral preprocessing results
图2. 光谱预处理结果
3.3. 模型建立
将预处理结果后的光谱数据与3.1项采样测得的淫羊藿药材总黄酮含量进行匹配,使用偏最小二乘法进行计算,得到如下表1。
通过比较发现,淫羊藿药材总黄酮含量模型通过进行光谱预处理处理后得到的模型相关系数R值更接近1,且有较低的RMSEC值,模型效果见图3。

Table 1. Total flavone content model parameters
表1. 总黄酮含量模型参数
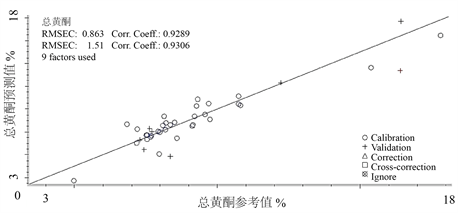
Figure 3. Schematic diagram of total flavone model of Epimedium
图3. 淫羊藿药材总黄酮模型示意图
3.4. 模型验证
3.4.1. 准确性
为了验证淫羊藿药材中总黄酮模型的准确性,利用建立的PLS模型对40个淫羊藿药材进行预测,并进行2.3项下对总黄酮进行含量测定,得到模型验证结果。从预测结果来看(如图4),预测值与真实值接近,符合中药分析的精度要求。用NIR定量校正模型验证淫羊藿总黄酮含量的预测效果优良。
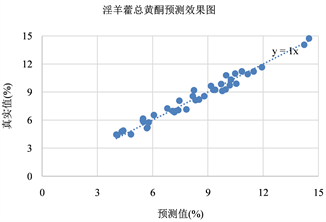
Figure 4. Prediction effect of total flavone of Epimedium
图4. 淫羊藿总黄酮预测效果图
3.4.2. 显著性
为进一步验证模型预测结果的准确性,将真实值与预测值含量数据进行独立样本T检验算法,评价测定结果的可靠性(如表2所示)。
从统计学的角度来看,P > 0.05,解释为没有足够的统计学证据来拒绝原假设,说明在这个样本中没有足够的证据去拒绝无差异的假设,即认为真实值与预测值之间无显著性差异。

Table 2. Paired samples t-test table
表2. 成对双样本均值的t-检验表
3.4.3. 差值的正态分布
画出直方图和正态分布的密度函数,并进行正态分布检验。
从图5上来看,两个分布具有相似的趋势,且检验得到的p值大于等于0.05,这表明我们未能拒绝原假设,即差值分布与正态分布之间没有显著差异。这结果表明我们的数据在差值方面呈现出与正态分布相似的特性。因此,我们可以合理地认为,在当前的分析中,差值的分布与正态分布之间没有显著性差异。
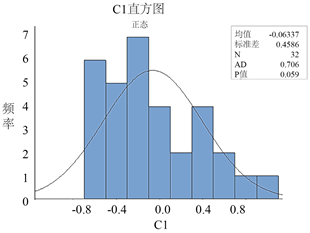
Figure 5. Normal distribution test histogram
图5. 正态分布检验直方图
结论:P > 0.05,差值的分布与正态分布没有显著性差异。
从上述三个角度来验证淫羊藿总黄酮模型,其结果均符合要求,可以用于检测淫羊藿总黄酮含量,实现淫羊藿质量的快速检测。
4. 结论
通过本研究,制定了一种用于淫羊藿药材中总黄酮含量的近红外快速分析方法。运用PLS建立了该含量的定量校正模型,相关系数R达到0.9289,RMSEP为0.863,满足了定量分析的标准。所构建的近红外模型能够在短时间内通过采集光谱对淫羊藿药材中总黄酮含量进行准确测定,相较于传统方法(HPLC),具备了简便、快速、无损的优势。
参考文献