1. 引言
现代医学认为感冒为多种病原体引发的急性上呼吸道感染,可引发黏膜充血水肿,产生鼻塞、咳嗽等上呼吸道炎性症状,并有头痛、恶寒发热等全身症状 [1] [2] 。中医认为感冒多见肺热亢盛,可出现肺失宣肃,甚至肺气郁闭的病理变化,疾病发展至后期又可出现肺之气阴耗伤或痰瘀阻滞肺络。中医治疗具有辨证论治的理念与方法:邪犯肺卫时,主以疏表透邪,并注意配合清宣肺热;肺热亢盛时,主以清宣肺热;肺气郁闭较甚者,则主宣肺、泻肺 [3] 。
复方感冒灵颗粒是由中药和化学药配伍组成的复方制剂,其中对乙酰氨基酚作为最常用的解热镇痛药之一,对发热、咽痛、全身酸痛等效果明显,且安全性高;此外还包含:马来酸氯苯那敏、咖啡因 [4] [5] 、山银花 [6] [7] 、五指柑 [8] 、野菊花 [9] [10] 、三叉苦 [11] 和岗梅 [12] [13] [14] [15] 等中药成分。复方感冒灵颗粒是将上述多种成分相结合,发挥药效间相互协同作用于人体,抵抗感冒病毒。目前,流行性感冒是由流感病毒引起的上呼吸道感染病,感冒具有易染病和流感范围广等特点 [16] [17] 。因此感冒药作为抗感冒药类中的疗效药,具有见效快和周期短等特点,在临床上广泛使用。但如不了解其中的药理特征及作用,极易用药不当 [18] [19] [20] ,而复方感冒灵颗粒作为能够有效治疗感冒的药品之一,其市场需求也是极为广阔。
目前中药生产缺乏基于过程分析技术(PAT)的质量在线检测与控制系统,因此虽然能获取产品生产过程工艺参数数据,但缺乏物料属性参数和质量指标参数数据 [21] 。近红外分析技术广泛应用在食品、烟酒、化学及中药领域,NIRs具有检测快,不破坏样品可同时反馈化学和物理信息的优点,因此可用于开发过程在线监控模型 [22] [23] [24] 。在复方感冒灵颗粒全过程生产工序中,浸膏工段已经是有效成分提取浓缩最后一道关卡。此时浸膏中密度为生产放行指标,由于浸膏在浓缩过程中存在不均一性、不稳定性,所以蒙化苷作为控制指标在此工序中的快速检测也就重中之重,因而为了提高中药制剂产品质量均一性和稳定性,实现浸膏质量快速评价和终点的快速判断十分迫切。在复方感冒颗粒的生产过程中,控制及监控蒙花苷含量成分是浸膏浓缩阶段的放行指标之一,因此蒙花苷的参数含量对最终成品药效起到至关重要的作用。
本研究利用NIRs技术快速无损采集复方感冒灵颗粒中浸膏光谱,并将化学计量学方法-偏最小二乘法与近红外光谱技术相结合,建立复方感冒灵颗粒浸膏中蒙花苷的定量分析模型,以期提供一种快速简便准确的检测方法,能够为复方感冒灵颗粒浸膏阶段放行提供数据支撑。
2. 实验部分
2.1. 仪器与试剂
复方感冒灵颗粒浸膏(华润三九(郴州)药业有限公司);MicroNIR PAT-U近红外光谱仪(北京格致同德科技有限公司);MS304TS型电子天平(梅特勒–托利多公司);色谱柱:Waters X Bridge® Shield RP18 (4.6*250 mm, 5 µm);Agilent1200高效液相色谱仪;
乙腈(HPLC, SIGMA-ALDRICH);纯净水(杭州娃哈哈集团有限公司);磷酸(色谱纯,上海阿拉丁生化科技股份有限公司);甲醇(色谱纯,天津市大茂化学试剂厂)。
2.2. 近红外漫反射光谱采集
复方感冒灵颗粒浸膏光谱采集预处理:根据浸膏工段收膏分装前,随机均匀间隔取样5~8个样品,一次取样20 mL;共取样6批。
光谱采集条件:采集浸膏过程样品的漫反射光谱,光谱扫描范围908 nm~1650 nm,扫描次数为100次,光纤透射式探头光程2 mm,积分时间30.8 ms;实验采用空气为参比进行光谱采集分析,见图1。

Figure 1. Original near-infrared spectrum of Compound Ganmaoling Granule extract
图1. 复方感冒灵颗粒浸膏近红外原始光谱
2.3. 复方感冒灵颗粒浸膏蒙花苷的测定
检测条件:色谱柱:Waters X Bridge® Shield RP18 (4.6*250 mm, 5 µm),流动相A:乙腈;B流体中的0.2%磷酸与水的比例为50:50。检测波长:334 nm。流速:1.0 mL/min。采样量:10 µL。柱子温度:30℃。洗脱40 min。按表1的梯度洗脱时间表进行洗脱。

Table 1. Timetable for gradient elution of monosine
表1. 蒙花苷梯度洗脱时间表
标准品溶液制备:分别精密称取0.1 g蒙花苷和0.8 g绿原酸标准品,分别使用甲醇定容10 mL容量瓶中,稀释100倍。充分溶解,配制成含绿原酸80 ug/mL、蒙花苷10 ug/mL的混合标准溶液。
供试品溶液制备:精密移取1.0 mL复方感冒灵颗粒浸膏样品。加入精密称取100 mL色谱纯甲醇,称重记录,400 W,45 Khz超声45 min,充分溶解,冷却至室温,称重,补足挥发的甲醇,混匀,过滤得到供试品溶液。
2.4. 数据处理与模型性能评价
本研究基于VIAVI公司MicroNIRTMPro数据分析软件算法进行采集和数据分析。在采集光谱过程中,仪器状态、环境温度及噪声等多方面因素对近红外光谱的影响,需要进行对光谱进行预处理如平滑、微分、基线校正或标准正态变换等。在对光谱预处理后使用VIAVI公司数据分析软件中偏最小二乘法(Partial Least Squares, PLS)进行分析,将复方感冒灵颗粒的浸膏的近红外光谱与高效液相色谱法测定的蒙花苷含量进行投影,建立线性关系,得到最终浸膏中蒙花苷的含量定量模型。
在利用不同预处理消除外界因素对光谱质量的影响后,使用PLS方法建模,其中使用交叉验证法(Leave-One-Out Cross Validation, LOOCV)计算交叉验证均方根误差(RMSECV),RMSECV数值最小时选定模型最佳因子数。模型性能评价是以建立定量模型后,计算其相关系数(R)、校正集预测均方根误差(RMSEC)、验证集预测均方根误差(RMSEP)和验证集相对偏差(RSEP)为评价标准。相关系数是模型验证的重要指标,相关系数越趋近1,说明模型预测效果越好。RMSEC和RMSEP值差值越小越好。其中验证集相对偏差通常控制在10%内,数值越低越好。
3. 结果与讨论
3.1. 复方感冒灵颗粒浸膏蒙花苷含量测定结果
在复方感冒灵颗粒生产过程中,浸膏中蒙花苷作为质量放行的重要的中药成分,无损快速测定生产批次浸膏蒙花苷药材含量是保证成品制剂安全有效的前提。按照2.3项下的测定方法,测定浸膏中蒙花苷含量,根据测定59个样品确定蒙花苷范围为1419.23~9426.74 ug/mL之间。
3.2. 光谱预处理
为了确保近红外光谱采集的稳定性和精确度,使用VIVIA数据分析软件中常用的光谱预处理方法有:正交信号校正(OSC)、一阶导数(1st derivative)、二阶导数(2nd derivative)、去趋势化(detrend)、矢量归一化(SNV)等。可以有效降低外界环境及仪器状态带给样品近红外光谱之间的差异,确保近红外光谱包含了样品大量的有效信息。本研究比较了不同预处理方法对复方感冒灵颗粒浸膏中蒙花苷含量建模的影响,选出了最佳建模参数,结果如表2所示。

Table 2. Model parameters of Mongolian glycoside content in Compound Ganmaoling Granules
表2. 复方感冒灵颗粒蒙花苷含量模型参数
通过比较发现,复方感冒灵颗粒浸膏蒙花苷含量模型通过SNV进行光谱预处理,预处理后的光谱将噪音及外界条件对光谱产生的影响进行删除,并提高有效信息在光谱中的体现,且相关系数R值更接近1,模型效果见图2。
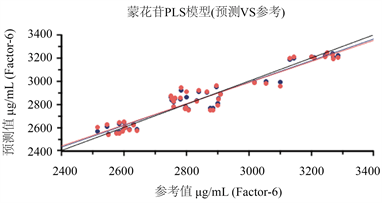
Figure 2. Schematic diagram of monglucin model of Compound Ganmaoling Granules
图2. 复方感冒灵颗粒蒙花苷模型示意图
4. 结论
本研究结合化学计量学PLS方法和NIRs技术,构建了复方感冒灵颗粒浸膏中蒙花苷含量快速测定的方法。通过建立的含量模型,可以实现复方感冒灵颗粒浸膏阶段的无损快速检测蒙花苷含量,并可以精准明确放行标准蒙花苷含量。通过相关系数及均方根误差的参数确定蒙花苷定量模型性能较好,具有较强的稳定性和准确性。
参考文献
NOTES
*通讯作者。