1. 引言
世界淡水总面积仅占地球表面积的0.8% [1],却分布着地球上近9.5%的物种 [2]。不协调的栖息地面积与物种丰富度导致淡水生态系统所面临生物多样性下降的风险远比陆地及海洋生态系统严重,而溪流生态系统通常会更具有脆弱性和敏感性 [3]。近年来全球气候变化、土地利用、外来物种入侵等对溪流生态系统的健康带来了极大的威胁。我国90%以上流经城市的溪流遭受污染,超过一半的主要城镇水源不适合饮用 [4]。
蜉蝣目,襀翅目和毛翅目(EPT)是大型底栖动物中对环境干扰非常敏感的三个类群,是监测淡水生态系统健康的常用指标之一 [5]。EPT是森林溪流生态系统的典型物种,是水生态系统食物链和食物网的重要环节,与其他水生昆虫共同在水生食物网中发挥重要作用 [6],将落叶、藻类等有机物碎屑与较高营养级联系起来 [7]。摄食功能群(Feeding functional groups, FFGs)是根据摄食对象和方法的差异对水生动物进行的一项生态分类 [8]。其强调的是大型底栖动物的取食策略 [9],这一生物特性在季节更替、栖息地改变及水生昆虫不同生长阶段均保持不变 [10],能更精确地表达不同水环境压力与大型底栖动物群落的之间的关系 [11]。
帽儿山国家森林公园位于黑龙江省尚志市东北林业大学帽儿山实验林场,近些年旅游业逐渐在帽儿山兴起,并对其生态资源和人文资源进行了开发。但公园内环境保护设施滞后,检测和评估体系较为缺乏 [12],生态环境遭受到了一定程度的影响。其中,为了使帽儿山溪流到达漂流效果,河道被重型机械挖掘,致使溪流堤岸岩石裸露,河道自然生境受到搅动和发生很大改变,部分河段渠道化(Channelize)。人为干扰带来的溪流渠道化造成了栖息地结构的改变,溪流周围生境类型趋于均质和破碎化。部分河段生境异质性程度降低,导致溪流重要的功能丰富度和多样性的减少或丧失 [13]。同时,溪流生境异质性改变会影响栖息在河道和河岸带等地的水生昆虫的多样性 [14],而要使其恢复到相对自然的状态需要花费很长时间 [15]。溪流的栖境受损严重,周围村屯居民生活也对帽儿山国家森林公园溪流生态系统带来一定的影响。然而EPT水生昆虫是对溪流环境非常敏感的类群,对水环境有特殊的要求,可以指示环境受干扰程度。因此,本文通过对帽儿山溪流EPT水生昆虫功能性状进行划分,探讨EPT在溪流的分布与水环境之间的关系,为帽儿山国家森林公园的保护提供依据。
2. 材料与方法
2.1. 研究地概况
帽儿山国家森林公园建园始建于1992年,隶属长白山系支脉,张广才岭西坡小岭余脉,平均海拔300 m,拥有典型温带大陆性季风气候 [16],在7~8月降水充沛。帽儿山溪流流经东北林业大学野外实习基地——帽儿山实验林场内(127˚30'~127˚34'E,45˚20'~45˚25'N),该溪流属于松花江一级支流阿什河的上游,其与帽儿山镇毗邻,周围零散分布着几个小型村屯,水质清澈见底,是帽儿山镇及各村屯居民的重要水源 [17]。而村庄生活污水、畜禽粪便等的倾倒,使帽儿山溪流面临水环境污染的威胁。此外作为旅游热点地区,缺少旅游项目检测和评估体系、改进与反馈机制等原因也使帽儿山溪流的自然生境受到旅游开发的影响。近年来,在帽儿山国家森林公园溪流开发旅游漂流活动,漂流河段主要分布于吕家围子、富民村、红明桥、头号桥区域,毗邻国道301景观带 [18]。
2.2. EPT的采集与鉴定
依据研究地所处气候条件,选择2019年春季在帽儿山溪流进行大型底栖动物的采集,并使用ArcGIS 10.3进行采样点示意图的绘制。根据溪流受到干扰程度的不同,划分为3个不同河段进行研究,分别为干扰段、恢复段和自然段(图1和表1)。其中,干扰段是指进行漂流的河段,位于研究河段的下游,共设置3个样点(S1~S3)。其中,S1距离村庄较近,河岸上正进行施工,岸边堆有河沙;S2、S3为漂流点,在水流较深、较急的夏季(7月和8月)会开展漂流活动。恢复段是指三年前曾经进行过漂流活动的河段,现由于某种原因已经废弃,处于自然恢复的过程中。恢复段位于研究河段的中游,共设置2个样点(S4~S5),其中S4与红明村毗邻,水较深,淤泥和有机腐殖质较多,有很多小卵石;S5溪流水体深度较S4浅,并且水质清澈,砾石和细沙较多。自然段指未受到认为干扰、环境较好的水体,位于研究河段的上游,共设置3个样点(S6~S8),溪流郁闭度大,远离村落,无人类干扰,其中S6水体腐殖质等沉积物较多;S7和S8水质清澈,水流较浅,但后者河道中具有较多的大块岩石,腐殖质也较多。
EPT昆虫的采集使用D型网(直径0.3 m,40目尼龙纱)进行,采样涉及到溪流不同的小生境,主要包括不同类型的底质(卵石、砾石、砂石、岩石、淤泥等)、枯枝落叶堆、倒木处、激流、静水区、泥沙沉积处等,每个样点采样总面积约为1 m2,并使用40目分样筛洗涤污泥,EPT昆虫在白瓷盘中进行现场挑选,之后存放入质量分数为85%的酒精中保存。
在实验室中使用Motic SMZ-168解剖镜将采集的EPT样本主要依据Morse J.C.等 [19]、周长发等 [20] 专业书籍,通过形态学的方式对照检索表和图谱将物种全部鉴定至属。
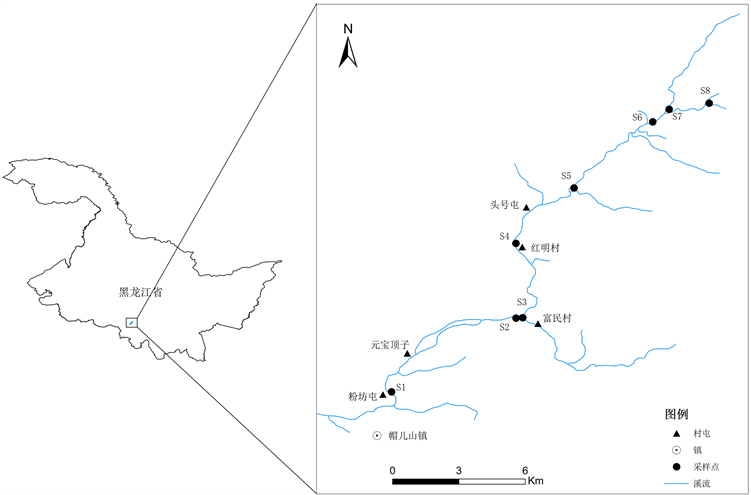
Figure 1. Sampling sites within streams of Maoershan National Forest Park
图1. 帽儿山国家森林公园溪流采样点示意图

Table 1. County level planning schedule
表1. 县域等级规划一览表
2.3. 栖境质量定性评价标准
参考Barbour等 [21] 和王备新 [22] 的方法以及评价标准,对不同河段采样点生境情况进行栖境质量定性评价。评价指标包括底质、栖境复杂性、静水区质量、堤岸稳定性、堤岸保护和覆盖度,并根据栖境的实际情况附上分值。评价标准:好:16~20,较好:11~15,一般:6~10,差:1~5。
2.4. 水体理化指标测定
在采集EPT样本的同时,使用YSI-6600多功能水质分析仪进行现场水体理化指标的测定,包括水温(WT, ℃)、电导率(Cond, us/cm)、浊度(Tur, NTU)。在每个采样点取水样500 ml带回实验室使用哈希DRB200消解仪和DR1900 COD试剂进行总磷(TP, mg/L)、总氮(TN, mg/L)和化学需氧量(CODCr, mg/L)的测定。
2.5. EPT功能群的划分
参考Yoshimura [7]、刘建康 [8]、Cummins [9] [23] 等对底栖动物摄食功能群的划分方法,根据水生昆虫的取食方法和策略,将其划分为直接集食者(Gather-collectors, GC)、刮食者(Scrapers, SC)、捕食者(Predators, PR)、杂食者(Omnicorous, OM)、过滤收集者(Filter-collectors, FC)和撕食者(Shredders, SH)等。
2.6. 数据处理
使用Canoco 5.0对EPT摄食功能群和水环境参数之间的关系进行冗余分析(RDA);使用SPSS 22.0进行单因素方差分析(One-way ANOVA)和多重比较,以检测溪流不同河段TP、TN、CODCr、WT、Cond、Tur的差异。
3. 研究结果
3.1. 不同河段栖境质量定性评价
对帽儿山国家森林公园溪流各河段进行栖境质量的定性评价(表2)。在干扰段(图2,A1, A2),溪流底质情况较好,砾石、卵石和较大的岩石占底质的1/2以上,但因为有石块被人工挖掘、岩石裸露等的原因,水体浑浊,泥沙也较多,所以在整体上没有达到一个很好的标准;栖境复杂性和覆盖度较差,因为人为修整河道,两岸乔木等大型植被缺乏,溪流几乎完全暴露在光线下;同时因为漂流需要,干扰段仅有急流而没有静水区;堤岸稳定性在富民村因为利用水泥对堤岸进行了加固,产生硬质河岸,侵蚀情况很少出现。
在恢复段(图2,B1, B2),底质情况在S4较好,但是在S5中细沙的比例较大,因而综合看来,恢复段底质情况未能在短时间得到很好的改善,仍处于较好评价;在S4处,溪流较深,水流较缓,在S5处有一个支流汇聚,河段具有一个沉积区,静水区质量一般;河道两岸的植被丰富,高大乔木众多,但因为有人工修建的造景存在并且占据了一定面积,因而堤岸稳定性、堤岸保护和覆盖度都只能处于较好。
在自然段(图2,C1, C2),底质中砾石、卵石和较大的岩石占3/4以上,情况较好;河道两岸植被丰富,并且具有巨石、倒凹堤岸等小栖境,因而栖境复杂性较好;在S6和S7河道非常宽,溪流浅,兼有深、浅静水区域,静水区质量好,并且靠近溪流处高大乔木比较少,堤岸稳定性、堤岸保护都仅处于较好状态,S7河道有被侵蚀的痕迹,但被侵蚀的面积不超过30%,堤岸稳定性属于较好;在S8处河道较窄,堤岸密生乔木和灌木,因而覆盖度综合看来较好。

Table 2. Qualitative Evaluation of habitat quality in different stream sections
表2. 不同河段栖境质量定性评价
3.2. 不同河段水环境理化因子分析
对帽儿山国家森林公园溪流各河段的水环境理化因子进行比较,并通过单因素方差分析来判断各河段之间水环境理化因子差异性是否显著(表3)。通过分析可知,在干扰段,所有理化参数均是最高的;恢复段的总磷(TP)、总氮(TN)最低;自然段的化学需氧量(CODCr)、水温(WT)、电导率(Cond)和浊度(Tur)为最低。除WT和Cond差异性显著外(p < 0.05),其他所有参数均无显著差异。
根据GB 3838-2002《地表水环境质量标准》,在干扰段S3中,CODCr为15.90 mg/L,处于II类和III类水标准之间;在所有河段中,TP和TN的含量均较高,在S3中TP甚至达到了6.90 mg/L,已经远超V类水标准。除此之外,S3的Tur高达284.20 NTU,样点处的水流非常浑浊,泥沙翻滚,水流急速,受漂流区域旅游开发的影响非常大。

Table 3. Water environmental factors (means ± standard deviations (SD)) and single factor analysis of variance (One-way ANOVA) in different stream sections
表3. 不同河段水环境理化参数及单因素方差分析
*注:表格内数据为平均值±标准差。
3.3. EPT物种组成与FFGs划分
此次调查共采集到EPT昆虫样本116头,13科15属(表4)。蜉蝣目(Ephemeroptera)的数量最多,共计83头,占EPT总数的71.6%,其中又以短丝蜉属(Siphlonurus)数量最多,占EPT总数的29.3%;襀翅目(Plecoptera)中Phanoperla属数量最多,占EPT总个体数的6.9%;而对于毛翅目(Trichoptera),Nemotaulius属数量最多,占EPT总个体数的12.1%。

Table 4. EPT list and functional feeding groups (FFGs) in Maoershan National Forest Park
表4. 帽儿山国家森林公园EPT名录及其摄食功能群
3.4. 不同河段EPT FFGs类型比较
大型底栖动物的取食行为与其周围环境可以提供的食物资源存在一定的关系,摄食功能群在对环境条件和变量上的评估具有重要的作用 [24]。对帽儿山国家森林公园不同河段的EPT摄食功能群密度分布进行统计(图3)。在干扰段和自然段中,GC都有明显的优势,其密度的最大值出现在自然段,为52个/m2,且均为蜉蝣目的种类;FC仅在恢复段中发现,且密度最小,为2个/m2;SC密度最大值出现在自然段,为14个/m2,而在干扰段和恢复段却较少或几乎没有分布;PR在恢复段的密度较大,为11个/m2。而在研究中所有河段均未见有OM和SH存在。
分别对三个河段的EPT数量和科属进行统计,结果为干扰段共计23头,隶属于7科7属;恢复段共计25头,隶属于6科6属;自然段共计68头,隶属于7科9属。自然段的物种数量是干扰段和恢复段的近3倍,科属分布也比较丰富,因而自然段的丰富度明显大于干扰段和恢复段;恢复段由于自然恢复的时间比较短,在物种数量和科属分布上与干扰段相比没有明显优势。人为干扰给溪流生态系统带来巨大的负面影响,为了实现漂流而对河道进行的人工拓宽、取直、挖掘大型石块等行为,使溪流渠道化,EPT的栖境遭受破坏。
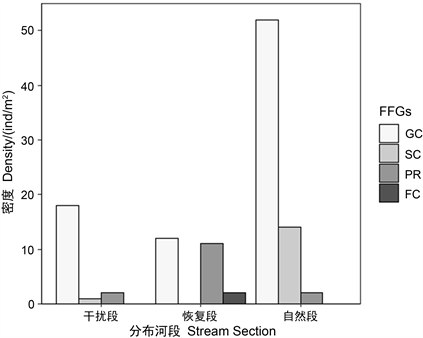
Figure 3. Density of feeding functional groups in different stream sections
图3. 不同河段EPT摄食功能群密度分布
3.5. EPT FFGs与水环境因子冗余分析
使用Canoco 5.0 对帽儿山国家森林公园EPT摄食功能群与水环境之间的关系进行分析,在分析前,对各水环境因子进行log(X+1)的变换,使其趋于正态分布。经软件进行除趋势对应分析后(DCA),发现物种数据的单峰响应值SD(梯度)为2.1,小于3,所以更适合使用冗余分析(RDA)。设置采样点为排序变量,EPT摄食功能群为响应变量,水环境变量为解释变量,作EPT摄食功能群与水环境因子的双序图(图4)。
RDA结果中显示(表5),前两轴的特征值分别为0.631和0.176,物种-环境相关性分别为0.904和1.000,并且物种累计变化率的80.6%在轴1和轴2中被解释。如图4所示,与轴1相关性较强的环境因子有WT (−0.272)和Tur (−0.281),并且由摄食功能群和水环境因子之间的夹角可知,GC与所有水环境因子之间均没有很强的相关性,在三个不同的河段都有分布;刮食者(SC)与TP表现出一定的负相关性,说明水环境中的TP浓度较高可能不适宜其分布;PR与Cond表现出正相关关系,说明其能够忍受电导率较高的水环境。
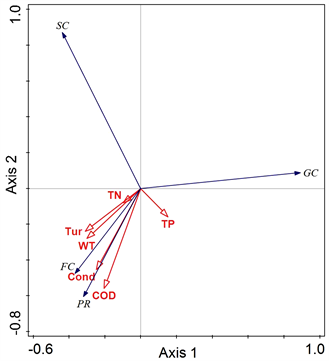
Figure 4. Biplots of EPT feeding functional groups and water environmental physical-chemical factors based on RDA ordination
图4. 基于冗余分析(RDA)的帽儿山国家森林公园EPT摄食功能群与水环境因子双序图

Table 5. RDA results for EPT feeding functional groups
表5. EPT功能群RDA分析结果
4. 讨论
淡水生态系统是世界上最易受影响和濒临灭绝的生态系统 [25],而山溪是最脆弱的生态系统,其水生昆虫等无脊椎动物物种多样性通常受到多种自然环境条件的限制,对人类干扰亦敏感,也被广泛用于研究淡水生物多样性和生物功能性状 [26]。水生昆虫具有种类多,生活周期长;活动场所比较固定,易于采集;不同种类对水质的敏感性差异大,受外界干扰后群落结构的变化趋势经常可以预测等特点,经常被作为反映溪流水环境变化的重要指示生物 [27]。
帽儿山国家森林公园溪流上游是大青山东坡尖石砬子沟,平均海拔311 m,流经红明村、进德村、富民村、元宝顶子、粉坊屯、帽儿山镇等村屯小镇,以及在溪流河口具有一段漂流景观带,与301国道毗邻 [18]。然而本次研究发现溪流受到严重的干扰,在粉坊屯、富民村是旅游的漂流河段,溪流堤岸被挖掘过,溪流基本都是细沙底质,水体浑浊,致使帽儿山溪流部分河段被渠道化,原本自然的溪流受到人类的改变。根据Timo Muotka等 [15] 的研究,渠道化导致溪流结构复杂性丧失,简化流动模式,同时也会降低一些生物微生境的可用性,而栖境异质性和复杂性的下降可能导致大型底栖动物生物多样性丧失 [28]。
在进行帽儿山溪流不同河段栖境质量进行定性评价中发现,在干扰段的溪流的栖境复杂性非常差,沿岸带仅零星斑块状分布一些莎草科植物,溪流两岸几乎没有高大的乔木和灌从分布,植被覆盖度非常低,而溪流中的大型底栖动物会受到溪流两侧林冠有无的强烈影响 [29]。除此之外,在刘曼红等 [30] 的前期研究中也发现,漂流活动因其会对溪流造成人为搅动的特性,也会对EPT昆虫的生存造成负面影响。
对帽儿山国家森林公园溪流不同河段(干扰段、恢复段和自然段)进行水环境理化因子的分析。从结果来看,在干扰段,由于受人为干扰较大,溪流环境受到一定程度的破坏,其所有理化参数数值均是最高的;恢复段包括红明桥和头号桥,前者与红名村相邻,但生境情况较好,栖境复杂性较高,溪流两岸是针阔混交林,同时灌木及莎草科植物丰富,覆盖度较高。此处CODCr比较高,但仍然处于GB 3838-2002《地表水环境质量标准》中的I类或II类水质标准;头号桥是一个漂流的废弃点,在河道一岸有木制港口造景,此外生境恢复较好,两岸为针阔混交林,溪水较浅,覆盖度高。自然段包括三号桥、十号桥和九号桥,溪流较浅,九号桥河宽较窄,但两岸覆盖度高,以阔叶乔木和灌木为主。自然段CODCr、WT、Cond和Tur为最低,单因素方差分析WT和Cond在不同河段有明显差异(p < 0.05),这与李强等 [31] 关于EPT的研究相似。而温度会对包括EPT在内的底栖动物群落结构组成造成一定的影响 [32],这可能是干扰段与自然段EPT群落组成存在差异有关,同时溪流自然段的温度偏低,与溪流两岸植被导致溪流的郁闭度较高、水体接受光照较少、高的海拔等因素有关。
摄食功能群(FFGs)是指生物的摄食策略,是生物的重要的功能性状。应用生物性状的方法可以预测某种环境胁迫对水生无脊椎动物(尤其EPT)生物群落的影响 [33],本研究发现的EPT的四种FFGs,其中直接集食者(GC)功能群在干扰段和自然段均具有明显的优势,为52个/m2,同时,使用RDA分析发现GC功能群与水环境中各因子均无很强的相关性,说明GC功能群不能很好地反应水质情况;PR与Cond表现出正相关关系,说明其能够忍受电导率较高的水环境;刮食者(SC)功能群与TP呈现负相关关系,结果均与李强等 [31] 的研究相似。滤食者(FC)功能群仅有一属Brachycentrus在恢复段中的头号桥出现,通过观察其巢穴,发现其巢材主要是粒径很小的沙粒,而在所有河段中,这样细密的沙粒仅在头号桥存在,且头号桥河道两岸为针阔混交林,覆盖度大,有足够的有机食物碎屑供给FC,与事实相符。
5. 结论
1) 在干扰河段,仅底质处于较好状态、堤岸稳定性处于一般状态,栖境复杂性、静水区质量、堤岸保护、覆盖度均很差;在恢复河段,仅静水区质量处于一般,其他各项指标均处于较好状态;在自然段,除了堤岸稳定性是较好之外,其他各项均处于好的状态。
2) 溪流干扰段、恢复段、自然段的水环境理化因子中,水温(WT)和电导率(Cond)在不同河段间差异性显著(p < .05),其中干扰段的化学需氧量(CODCr)、总磷(TP)、总氮(TN)值均最高,且CODCr超过地表水环境质量标准中的II类,水体呈现富营养化趋势。
3) 共鉴定出EPT水生昆虫13科15属,共计116头,划分出4个摄食功能群类型,分别为GC、SC、PR和FC,其中GC广泛分布于3个河段,在自然段其密度最大,为52个/m2。
4) RDA分析表明,GC与所有水环境因子之间均没有很强的相关性;SC与TP表现出一定的负相关性;PR与Cond表现出正相关关系。
致谢
本研究的采样阶段由东北林业大学孟昭军教授、本科生张韵协助完成。
基金项目
东北林业大学创新创业计划项目,项目编号:201910225254。
NOTES
*通讯作者。