1. 引言
作为生物体内最重要的元素之一,氮元素是构成核酸和氨基酸的基本成分之一,对地球上的生命体意义不言而喻 [1] [2] 。氨合成是自然固氮的重要反应,但是工业固氮需要大量的能量和氢气,动力学复杂,而且N2到NH3的转化涉及多电子反应。因此,寻找一种可以常温常压下无H2催化生产NH3且对环境友好的固氮工艺是非常必要的 [3] [4] 。在绿色固氮工艺中,光催化固氮得到研究者的关注。
通过光催化剂可以使N2变换为铵根离子,以及在半导体光催化剂中植入大量氧空位,并且实现将氧空位拓展到其它金属氧化物中,可以得到广泛的使用。光催化固氮技术,是一种新型的固氮形式就成为了科学研究中的重要课题 [5] 。ZnO作为半导体的催化剂,具有较高的光电转化效率,在光催化领域受到广泛关注。然而,ZnO催化剂也存在一些缺点,如光生电子和空穴易复合 [6] 。而且Ru具有很强的捕获光生电子的能力 [7] 。可以将ZnO导带上的光生量子转移到金属Ru上 [8] ,同时可以抑制光生电子与光生空穴的复合 [9] 。钌复合可以很明显的提高光催化的稳定性,并且Ru元素具有特殊的电子结构和光谱性质 [10] 。通过对ZnO进行形貌调控 [11] ,还可以改善光化学性能 [12] ,这探究了在可见光照射下光催化固氮性能,是实现光催化固氮的关键点。但是其光催化性能仍然存在由于电子–空穴对复合较快、比表面积小等造成的限制,这就意味着催化性能仍然可以有提高的空间 [13] 。在催化剂中构建丰富的光催化固氮活性位点,来促进N2的吸附和活化。因此,寻求高效的催化剂并对其进行改性以提升其光催化性能尤为重要。通过表面负载贵金属拓宽可见光吸收范围,提高光催化活性。
为了改变ZnO光催化的缺陷,改变其光催化固氮性能,通过金属钌复合的方式对Ru复合ZnO的催化剂进行改性。通过制备Ru复合ZnO的催化剂,控制加入Ru的含量,检测Ru复合ZnO的催化剂固氮性能,用XRD、紫外可见漫反射、电化学分析等对催化剂进行了表征,并对催化剂物相、吸光性能、阻抗等进行分析,表明了催化剂固氮的原因。
2. 实验部分
2.1. 试剂及设备
主要试剂和设备见表1和表2。

Table 1. County level planning schedule
表1. 主要试剂

Table 2. County level planning schedule
表2. 主要设备
2.2. 催化剂的制备
将0.72 g ZnSO4∙7H2O和0.074 g RuCl3∙xH2O溶于25 mL水中,再倒入250 mL容量瓶中,放入转子,根据化学方程式的关系算出需要的NaOH和NaBH4的量,NaOH的量要过量。NaBH4加入的物质的量是RuCl3∙xH2O物质量的5倍,在200 r/min搅拌转速和353 K还原温度下搅拌20 min,将25 mL 0.056 mol/L NaBH4溶液和25 mL 0.234 mol/L NaOH溶液分别倒入上述溶液中,倒完后再搅拌20 min。然后对得到的物质进行减压抽滤,最后趁热过滤,用蒸馏水洗涤至过滤的液体为中性。将的得到的催化剂放在烘箱中于60℃下干燥两个小时,研磨成粉状,最后可以得到Ru复合ZnO的催化剂。改变催化剂的制备方法,对ZnSO4∙7H2O与RuCl3∙xH2O的物质的量的比例改变,探索出最好的一组比例。则ZnSO4∙7H2O与RuCl3∙xH2O的物质的量比例分别为:9:1、8:2、7:3、9.5:0.5、9.25:0.75,得到一系列不同溶质比下制备的Ru复合ZnO的催化剂,所加入的试剂与上述计算方法一致。在最优ZnSO4∙7H2O与RuCl3∙xH2O的比例下,调控反应的温度,考察反应温度对光催化固氮性能的影响。控制变量在最优比例下一个不加入硼氢化钠,一个加入的硼氢化钠的量是RuCl3∙xH2O物质的量的十倍,并进行实验。
2.3. 铵根离子检测方法
纳氏试剂是由碱性溶液(NaOH或者KOH)中的二价汞碘化物和碘化钾组成,当加入含有低浓度氨的溶液中,会产生黄色的复合物,并形成胶体溶液,检出限为28 × 10−6M,总反应式如下式:
分别配置0.0 μg/mL、0.1 μg/mL、0.15 μg/mL、0.20 μg/mL、0.40 μg/mL、0.60 μg/mL、0.80 μg/mL、1.0 μg/mL铵离子标准溶液,在上述溶液中分别加入1 mL 0.38 mol/L的酒石酸钾钠溶液,加入1 mL纳氏试剂,进行搅匀静置20 min。利用紫外分光光度计,用去离子水进行校零,分别测量在420 nm的吸光度为纵坐标,横坐标为溶液NH4+浓度,紫外吸光度曲线和标准曲线见图1(a)和图1(b),标准曲线的拟合公式为:

Figure 1. UV absorbance curves (a) ammonium chloride standard curves (b)
图1. 紫外吸光度曲线图(a)氯化铵标准曲线图(b)
2.4. 催化剂固氮测试
用量筒量取100 mL蒸馏水,量取0.1 g Ru掺杂的ZnO的固体催化剂放入固氮装置中,调节转速为420 r/min,在室温298 K下进行反应。开始计时,先暗反应进行半个小时,半小时后取一次样,暗反应结束后,然后打开LED大功率光源,再每隔半小时取一次样,光照下取四次,总共取五次样,取样后用1 mL移液管依次加入0.2 ml 2.381 mol/L酒石酸钾钠溶液和0.2 mL钠氏试剂。纳氏试剂比色法具有操作简单,灵敏度高的优点,但是该方法会受到一些金属离子的干扰,因此需要在加纳氏试剂前先添加酒石酸钾钠,作为掩蔽剂,以减少这些离子的干扰。放完试剂后,用离心机离心一分钟,转速10,000 r/min,离心后,用紫外吸收光谱仪器检测吸光度,调整测定时的吸收波长为420 nm,然后用超纯水进行校零,最后进行吸光度的检测,可以根据标准曲线图来计算固氮率。
2.5. 催化剂表征
XRD的检测:使用日本理学株式会社的X射线衍射仪,型号为Ultima Ⅳ,测试条件为:扫描使用CuKα射线,射线的波长为0.15418 nm,管电压40 kV,管电流为40 mA。扫描范围2θ为10~90˚。采用UV-Vis光度计(ThermoNicolet公司制造,Cary-5000)扫描样品来测试吸收性能,扫描波长200~800 nm。结合电化学工作站进行分析。
3. 结果与讨论
3.1. 不同含量Ru复合ZnO的XRD表征
图2为不同含量Ru复合ZnO的XRD图。可以看出,纯ZnO的催化剂在2θ = 33˚、35˚、48˚处显示出Zn4O3(SO4)∙7H2O特征衍射峰,在2θ = 36˚出现立方相ZnO的衍射峰。随着Ru复合量的增加,样品Zn4O3(SO4)∙7H2O特征衍射峰半高宽逐渐增大,说明Ru复合使Zn4O3(SO4)∙7H2O微晶尺寸越来越小。且Ru复合后并未出现Ru物种的特征衍射峰,说明Ru物种的微晶尺寸很小。
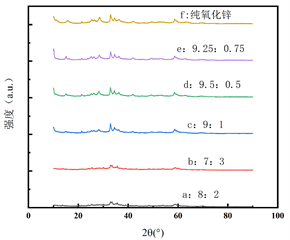
Figure 2. XRD patterns of ZnO composited with the different Ru contents
图2. 不同含量Ru复合ZnO的XRD谱图
3.2. 不同含量Ru复合ZnO的紫外–可见漫反射表征

 (a) (b)
(a) (b)
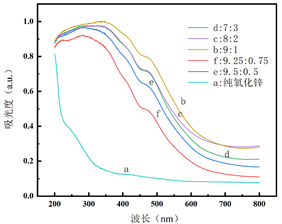
Figure 3. UV diffuse reflectance spectrum (a) and band gap diagram (b) of ZnO composited with the different Zn contents
图3. 不同含量Ru复合ZnO紫外漫反射光谱图(a)和能带间隙图(b)
图3(a)给出了不同含量Ru复合ZnO的紫外漫反射光谱图。可以看出,随着Ru复合量的增加,吸收光的波长向长波方向移动,长波即为可见光区,且吸收光的强度增加。因为加入金属Ru后,催化剂的颜色加深,敏化了ZnO,吸收光的范围扩大,强度增加。图3(b)给出不同含量Ru复合ZnO的带隙图。可以看出,Ru复合氧化锌的禁带宽度逐渐变小,说明Ru组分敏化了ZnO半导体,扩展了催化剂的波长响应范围,提高了催化剂吸收光的强度。
3.3. 不同含量Ru复合ZnO的电化学表征
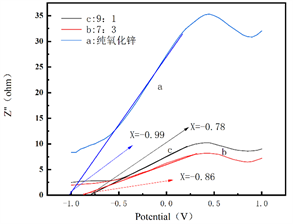
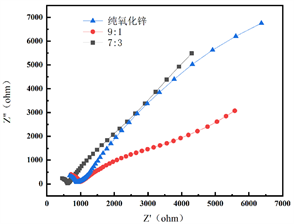
图4给出了不同含量Ru复合ZnO的EIS图。可以看出,9:1的比例下曲线半径最小,说明光催化剂电子转移的阻力最小,表明光生电子与空穴越易分离,光催化剂性能越佳。Ru复合ZnO催化剂的圆弧半径明显小于纯ZnO,表示Ru复合ZnO催化剂的电荷转移阻力减小,光生电子移动速度快于纯ZnO,使光生电子不与空穴发生复合,越容易进行固氮,这说明在这个比例下制备的催化剂的表面有利于电荷的传输和光生载流子传递效率的提高,因此,该比例下制备的催化剂的表面有利于光生电子与空穴分离的效率提高,催化剂性能最佳。图4(b)给出了不同含量Ru复合ZnO的莫特–肖特基图。可以看出,纯氧化锌及Ru与Zn的比例为9:1和7:3的平带电位(EFB)分别是−0.99 V、−0.78 V、−0.86 V。纯氧化锌的平带电位最小,其还原能力最强。
 (a) (b)
(a) (b)
Figure 4. EIS diagram (a) and Mott Schottky curves of ZnO composted with the different Ru contents
图4. 不同含量Ru复合ZnO的EIS图(a)和莫特–肖特基图(b)
3.4. 不同含量Ru复合ZnO固氮性能

Figure 5. Nitrogen fixation performance of ZnO composited with the different Ru contents
图5. 不同含量Ru复合ZnO固氮性能图
图5不同含量Ru复合ZnO固氮性能图。可以看出,随着Ru复合量的增加,ZnO催化剂的固氮性能增加。随Ru复合量的增加,催化剂带隙变小,催化剂吸光能力增加,光生电子转移速率增大,催化剂的固氮性能增加。催化剂在9:1的制备中固氮性能最好。再增加Ru的含量,催化剂的固氮性能降低,这可能是由于Ru物种团聚引起的。
3.5. 不同硼氢化钠浓度制备Ru复合ZnO的XRD表征
图6给出了不同硼氢化钠浓度制备Ru复合ZnO的XRD图。可以看出,随NaBH4浓度增加,ZnO的特征衍射峰强度逐渐增加,说明硼氢化钠的用量会影响到ZnO的粒径。随NaBH4浓度增加,制备的催化剂上并未发现金属Ru的特征衍射峰,说明Ru的粒径很小。
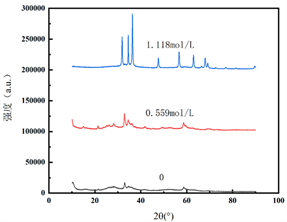
Figure 6. XRD patterns of ZnO composited with Ru prepared under the different NaBH
图6. 不同硼氢化钠浓度制备Ru复合ZnO的XRD图
3.6. 不同硼氢化钠浓度制备Ru复合ZnO的紫外–可见漫反射表征
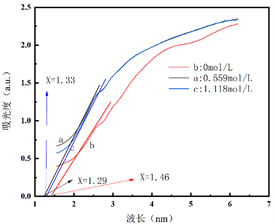
 (a) (b)
(a) (b)
Figure 7. UV diffuse reflectance spectrum (a) and band gap diagram (b) of ZnO composited with Ru prepared with the different NaBH4 concentrations
图7. 不同硼氢化钠浓度制备Ru复合ZnO的紫外–可见漫反射图(a)和能带间隙图(b)
图7(a)给出了不同硼氢化钠浓度制备Ru复合ZnO的紫外可见漫反射图。可以看出,随硼氢化钠浓度增加,吸收光的波长向可见光区移动,且吸收强度增加。然而继续增加NaBH4浓度,催化剂的吸光强度反而减小。图7(b)给出了不同NaBH4浓度制备Ru复合ZnO的能带间隙图。可以看出,增大硼氢化钠的浓度,禁带宽度减小,吸收光强度增大。然而继续增加NaBH4浓度,催化剂能带见习反而增大,吸光强度减小。
3.7. 不同硼氢化钠浓度制备Ru复合ZnO的光催化固氮性能
图8给出了不同浓度硼氢化钠制备Ru复合ZnO光催化固氮性能图。由图可知,随着硼氢化钠的浓度增加,铵根离子浓度先增加后减小,最佳的硼氢化钠浓度为0.559 mol/L。由表征可知,硼氢化钠浓度为0.559 mol/L时制备Ru复合ZnO催化剂,吸光性能最佳,带隙最小,催化剂固氮性能最佳。

Figure 8. Nitrogen fixation performance of ZnO composited with Ru prepared with the different NaBH4 concentrations
图8. 不同浓度硼氢化钠制备Ru复合ZnO光催化固氮性能图
3.8. 不同干燥温度下制备的Ru复合ZnO的固氮性能
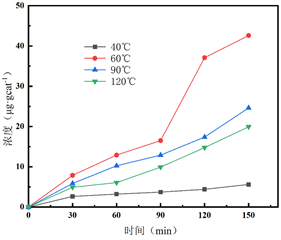
Figure 9. Nitrogen fixation performance of ZnO composited with Ru prepared under the different drying temperatures
图9. 不同干燥温度下制备的Ru复合ZnO的固氮性能图
图9给出了不同干燥温度下Ru复合ZnO的固氮性能图。由图可知,随干燥温度升高,Ru复合ZnO光催化固氮性能逐渐增加,这可能是由于干燥温度升高Ru复合ZnO的晶型趋于完整,光催化的性能较高。当干燥温度为60℃,催化剂固氮性能可达8.52 μg∙gcat−1。继续升高温度,Ru复合ZnO固氮性能反而降低。这可能是由于干燥温度过高,使催化剂活性组分团聚而导致的。
4. 结论
用沉淀还原法制备了Ru复合ZnO光催化剂。随着Ru复合量的增加,吸收光的波长向可见光区移动,且吸收光的强度增加,能带间隙减小,光生电子与空穴分离的效率提高,光生电子转移速率加快。当ZnO与Ru的物质的量之比为9:1时,加入的硼氢化钠的浓度为0.056 mol/L,干燥温度为60℃时,所制备的Ru复合ZnO催化剂的光催化固氮性能最佳,为8.52 μg∙gcat−1。
基金项目
河南省大学生创新创业训练计划项目(202312949003),郑州师范学院大学生创新创业训练计划项目(DCZ2022013)。
参考文献
NOTES
*通讯作者。